
Organiske forbindelser
Nomenklatur
Nomenklaturens opbygning
Navngivningen af organiske forbindelser er bygget op over et relativt stringent regelsæt, som man følger til en vis grænse. Dette skal forstås på den måde, at man i den systematiske navngivning kan komme ud for at have flere valgmuligheder for navngivningen. IUPAC som står for systemet for navngivning har selvfølgelig sine favoritter, men det er ikke et krav at man følger IUPAC's anbefalinger. Der er kun ét krav til den systematiske navngivning: den skal være entydig.
Principelt er det muligt at lave systematiske navne til alle organiske molekyler, men virkeligheden er en noget anden, fordi der kommer et punkt hvor den systematiske navngivning bliver for tung at arbejde med, og man bruger en workaround. Denne workaround bliver gennemgået længere nede på siden. Navngivningen af et organisk molekyle foregår efter følgende liste:
Bemærk:
Navne på kæder findes her, navne på funktionaliteter og funktionelle grupper findes her.
Principelt er det muligt at lave systematiske navne til alle organiske molekyler, men virkeligheden er en noget anden, fordi der kommer et punkt hvor den systematiske navngivning bliver for tung at arbejde med, og man bruger en workaround. Denne workaround bliver gennemgået længere nede på siden. Navngivningen af et organisk molekyle foregår efter følgende liste:
- Den længste kæde af C-C-bindinger (herunder også dobbel- og trippelbindinger) er molekylets hovedkæde (stamhydridet), MEN:
- Hvis der er en funktionel gruppe, vil kæden med den funktionelle gruppe automatisk være molekylets hovedkæde.
- Hvis der er flere funktionelle grupper, vil kæden der indeholder flest funktionelle grupper være hovedkæden.
- Hvis der er flere kæder med samme antal funktionelle grupper, følges den prioriterede liste for funktionelle grupper.
- Dobbel- og trippelbindinger angives. Hvis der er Z/E- eller cis/trans-isomeri, skal dette også angives.
- Find de funktionelle grupper der måtte være på hovedkæden. Den hovedfunktionelle gruppe (gruppen der står højest på prioriteringslisten i listen med funktionelle grupper) vil bestemme endelsen (suffix) på navnet, og de øvrige funktionelle grupper der måtte være, kommer til at stå som præfix. Positionen for den funktionelle gruppe bestemmer nummereringen af de andre carbonatomer.
- Find sidekæder. Sidekæder benævnes alfabetisk, hvis der er mere end én og de er forskellige. Ved cykliske forbindelser defineres cis/trans-isomeri i forhold til ringen, ud fra den hovedfunktionelle gruppe.
- I tilfælde af optisk isomeri skal dette på som det sidste.
Bemærk:
- Hvis navnet indeholder tal til angivelse af placeringer og sammensatte sidekæder, adskilles disse med bindestreger og parenteser for at kunne overskue navnet f.eks. 3-(2-oxocyclohexyl)propansyre.
- Er der flere af samme funktionelle gruppe, adskilles de to positioner med komma, også selv om det er den samme position.
- Er der flere placeringer med cis/trans- eller Z/Eisomeri, nævnes de i samme rækkefølge som placeringerne af funktionaliteten.
Navne på kæder findes her, navne på funktionaliteter og funktionelle grupper findes her.
Længste kæde med C-C-bindinger
Som udgangspunkt søger vi den længste C-C-kæde, også kaldet stamhydridet, dog med det forbehold, at hvis der er flere funktionelle grupper på en kortere kæde, kommer denne til at dominere. Den problematik vender vi tilbage til længere nede. For at starte med det simple, så hedder dette molekyle ethan:
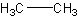
Der er 2 carbon, og kun enkeltbindinger. Hvis vi i stedet har 6 carbon,

hedder således hexan (6 carbon = hex). Hvis kæderne er lineære, kalder man det for alifater.
Kæderne behøver ikke være lineære. Hvis de er ringformede, kalder man det cykliske forbindelser eller aromater, afhængig af opbygningen. Aromater har kun konjugerede dobbeltbindinger i ringformationen, så de bliver er flade, cykliske forbindelser kan indeholde dele med konjugerede dobbeltbindinger, men er ikke flade:
Hvis atomerne i molekylet danner en ring tilføjer man cyclo foran kæden. Molekylet
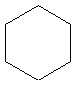
hedder således cyclohexan.
For lige at foregribe begivenhedernes gang, så har man cykliske forbindelser, som har en udbredelse og kompleksitet, så de har fået deres eget navn. Det er f.eks. crown ethere.
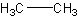
Der er 2 carbon, og kun enkeltbindinger. Hvis vi i stedet har 6 carbon,

hedder således hexan (6 carbon = hex). Hvis kæderne er lineære, kalder man det for alifater.
Kæderne behøver ikke være lineære. Hvis de er ringformede, kalder man det cykliske forbindelser eller aromater, afhængig af opbygningen. Aromater har kun konjugerede dobbeltbindinger i ringformationen, så de bliver er flade, cykliske forbindelser kan indeholde dele med konjugerede dobbeltbindinger, men er ikke flade:
Hvis atomerne i molekylet danner en ring tilføjer man cyclo foran kæden. Molekylet

hedder således cyclohexan.
For lige at foregribe begivenhedernes gang, så har man cykliske forbindelser, som har en udbredelse og kompleksitet, så de har fået deres eget navn. Det er f.eks. crown ethere.
Bindinger
Endelsen på navnet på en kæde afspejler om den indeholder enkelt-, dobbelt- eller trippelbindinger. Endelserne er:
Hvis vi har 2 carbon, kan vi have alle tre bindingstyper:
Som det ses, kan dobbelt og trippelbindingerne kunne sidde ét sted. En angivelse af placeringen vil derfor være overflødig. Hvis vi kommer op i en C4-kæde, bliver det aktuelt med en placering. Her kan dobbelt- og trippelbindingerne sidde mellem position 1 og 2 eller 2 og 3, så det angiver vi som hhv. 1-en og 2-en og 1-yn og 2-yn:
Reglerne for navngivning blev lavet om i 1990'erne, så man vil stadig kunne finde referencer med den gamle navngivning. Her satte man positionen af bindingen før kædelængden, dvs. de fire viste molekyler kom til at hedde 1-buten, 2-buten, 1-butyn og 2-butyn. Den nye systematiske navngivning er ikke så fonetisk velfungerende som den gamle, så de gamle systematiske navne som f.eks. 2-propanol i stedet for propan-2-ol, bruges stadig.
Er der flere dobbelt- eller trippelbindinger, adskilles positionen med komma, og man giver endelsen præfixet di, tri, osv. Dette molekyle:

kommer således til at hedde penta-1,4-dien.
- an = kun enkeltbindinger
- en = en eller flere dobbeltbindinger
- yn = en eller flere trippelbindinger
Hvis vi har 2 carbon, kan vi have alle tre bindingstyper:
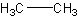 |  | 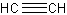 |
| ethan | ethen | ethyn |
Som det ses, kan dobbelt og trippelbindingerne kunne sidde ét sted. En angivelse af placeringen vil derfor være overflødig. Hvis vi kommer op i en C4-kæde, bliver det aktuelt med en placering. Her kan dobbelt- og trippelbindingerne sidde mellem position 1 og 2 eller 2 og 3, så det angiver vi som hhv. 1-en og 2-en og 1-yn og 2-yn:
 |  |  |  |
| but-1-en | but-2-en | but-1-yn | but-2-yn |
Reglerne for navngivning blev lavet om i 1990'erne, så man vil stadig kunne finde referencer med den gamle navngivning. Her satte man positionen af bindingen før kædelængden, dvs. de fire viste molekyler kom til at hedde 1-buten, 2-buten, 1-butyn og 2-butyn. Den nye systematiske navngivning er ikke så fonetisk velfungerende som den gamle, så de gamle systematiske navne som f.eks. 2-propanol i stedet for propan-2-ol, bruges stadig.
Er der flere dobbelt- eller trippelbindinger, adskilles positionen med komma, og man giver endelsen præfixet di, tri, osv. Dette molekyle:

kommer således til at hedde penta-1,4-dien.
Z/E - og cis/trans-isomeri
Dobbeltbindinger og cykliske forbindelser er låste i deres rotation, og man får en relativ orientering af op og ned, hvis der er 2 eller flere substituenter der skal positioneres. Hvis et molekyle er tegnet således:
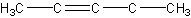
kan man ikke se forskellen, men hvis molekylet er tegnet således, med en lidt mere korrekt fremstilling af den tredimensionelle struktur:
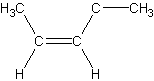
kan man se, at der er en forskel på om de to carbonatomer ved siden af dobbeltbindingen sidder på samme side af dobbeltbindingen, dette hedder cis eller Z. Hvis de sidder på hver sin side, dvs. på denne måde:
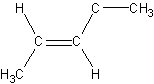
hedder det trans eller E.
Tilsvarende kan man se på de to isomerer af cyclohexan-1,2-diol:
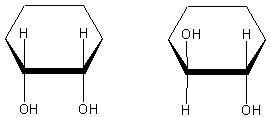
Venstre: cis-cyclohexan-1,2-diol. Højre: trans-cyclohexan-1,2-diol. (suffixet ol refererer til den funktionelle gruppe alkohol (-OH). Alkoholer og andre funktionelle grupper gennemgås i næste sektion).
Bemærk, at for cykliske forbindelser bruger man kun cis/trans. Det er en af forskellene på cis/trans og Z/E, og der er flere, så lad os starte med at få det på plads, for det er vigtigt.
Z/E og cis/trans udfylder den sammen funktion, men der er fundamentale forskelle, og de to nomenklaturer kan ikke helt det samme. Der vil derfor være molekyler, hvor man kun kan bruge den ene af de to nomenklaturer. Z står for zusammen (dvs. sammen) og E står for entgegen (dvs. imod, i betydningen modsat). cis er latin for på denne side og trans er latin for på den anden side.
Så, hvis vi ser på på dette molekyle:
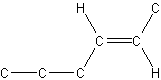
så kommer det til at hedde (E)-hex-2-en (ny nomenklatur) eller trans-hex-2-en (gammel nomenklatur).
Hvis der er flere dobbeltbindinger som f.eks.
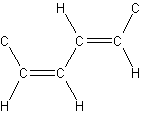
bliver det således til (Z,E)-hexa-2,4-dien (ny nomenklatur), eller cis,trans-hexa-2,4-dien (gammel nomenklatur), fordi den første dobbeltbinding, på 2-positionen, er Z/cis og den anden, på 4-positionen, er E/trans.
Visse steder foretrækker man at specificere Z/E-positionerne, f.eks. (2Z,4E)-hexa-2,4-dien. Hvis der kan være tvivl hvilket Z og E der hører til hvor, skal positionen selvsagt med, for at gøre navnet entydigt, men ellers kan angivelsen af positionen udelades.
Fordi der er en forskel på cis/trans- og Z/E-isomerien, så lad os tage et eksempel hvor man kan se forskellen:
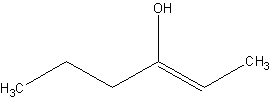
Ved cis/trans sidder de to carbon i trans-position, så efter cis/trans-nomenklaturen er molekylet (trans)-2-Hexen-3-ol. Efter Z/E-nomenklaturen er atomerne i de fire positioner omkring dobbeltbindingen er rangeret efter deres placering i det periodiske system, og oxygenet har et højere nummer end carbon, så de to højest rangerende atomer på hver side af dobbeltbindingen har samme orientering, dvs. Z, og molekylet kommer til at hedde (Z)-2-Hexen-3-ol. Så, for cis/trans-nomenklaturen er det en trans-forbindelse, men for Z/E-nomenklaturen er forbindelsen det der svarer til en cis-forbindelse.
Ved cykliske forbindelser betragter man ringen som atomerne udspænder som et plan, og man orienterer cis og trans i forhold til ringens plan. Z/E-nomenklaturen bruges ikke til cykliske forbindelser. Et molekyle som dette
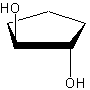
hedder således trans-cyclopentan-1,2-diol (suffixet ol refererer til den funktionelle gruppe alkohol (-OH). Funktionelle grupper bliver gennemgået i det næste afsnit).
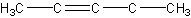
kan man ikke se forskellen, men hvis molekylet er tegnet således, med en lidt mere korrekt fremstilling af den tredimensionelle struktur:

kan man se, at der er en forskel på om de to carbonatomer ved siden af dobbeltbindingen sidder på samme side af dobbeltbindingen, dette hedder cis eller Z. Hvis de sidder på hver sin side, dvs. på denne måde:

hedder det trans eller E.
Tilsvarende kan man se på de to isomerer af cyclohexan-1,2-diol:

Venstre: cis-cyclohexan-1,2-diol. Højre: trans-cyclohexan-1,2-diol. (suffixet ol refererer til den funktionelle gruppe alkohol (-OH). Alkoholer og andre funktionelle grupper gennemgås i næste sektion).
Bemærk, at for cykliske forbindelser bruger man kun cis/trans. Det er en af forskellene på cis/trans og Z/E, og der er flere, så lad os starte med at få det på plads, for det er vigtigt.
Z/E og cis/trans udfylder den sammen funktion, men der er fundamentale forskelle, og de to nomenklaturer kan ikke helt det samme. Der vil derfor være molekyler, hvor man kun kan bruge den ene af de to nomenklaturer. Z står for zusammen (dvs. sammen) og E står for entgegen (dvs. imod, i betydningen modsat). cis er latin for på denne side og trans er latin for på den anden side.
- Til cykliske forbindelser kan man kun bruge cis/trans. Her refererer cis og trans til om de funktionelle grupper sidder på samme side af det plan som ringen udspænder, eller de sidder på hver sin side.
- For dobbeltbindinger orienterer cis/trans efter placeringen af 2 atomer af samme type, på hver sin side af dobbeltbindingen. Typisk er det carbon, men kan også være andet, f.eks. 2 hydroxygrupper. Er der ikke to atomer af samme type på hver sin side af dobbeltbindingen, kan man ikke bruge cis/trans, men skal bruge Z/E i stedet.
- Z/E orienterer efter atomernes postion i det periodiske system (Cahn-Ingold-Prelog- eller CPI-prioriteringen), så denne nomenklatur kan håndtere dobbeltbindinger med 3 eller 4 forskellige atomer på dobbeltbindingerne.
- cis/trans kan ikke håndtere specielle konstruktioner som f.eks. cumulener. Her skal man bruge Z/E-nomenklatur.
Så, hvis vi ser på på dette molekyle:

så kommer det til at hedde (E)-hex-2-en (ny nomenklatur) eller trans-hex-2-en (gammel nomenklatur).
Hvis der er flere dobbeltbindinger som f.eks.

bliver det således til (Z,E)-hexa-2,4-dien (ny nomenklatur), eller cis,trans-hexa-2,4-dien (gammel nomenklatur), fordi den første dobbeltbinding, på 2-positionen, er Z/cis og den anden, på 4-positionen, er E/trans.
Visse steder foretrækker man at specificere Z/E-positionerne, f.eks. (2Z,4E)-hexa-2,4-dien. Hvis der kan være tvivl hvilket Z og E der hører til hvor, skal positionen selvsagt med, for at gøre navnet entydigt, men ellers kan angivelsen af positionen udelades.
Fordi der er en forskel på cis/trans- og Z/E-isomerien, så lad os tage et eksempel hvor man kan se forskellen:

Ved cis/trans sidder de to carbon i trans-position, så efter cis/trans-nomenklaturen er molekylet (trans)-2-Hexen-3-ol. Efter Z/E-nomenklaturen er atomerne i de fire positioner omkring dobbeltbindingen er rangeret efter deres placering i det periodiske system, og oxygenet har et højere nummer end carbon, så de to højest rangerende atomer på hver side af dobbeltbindingen har samme orientering, dvs. Z, og molekylet kommer til at hedde (Z)-2-Hexen-3-ol. Så, for cis/trans-nomenklaturen er det en trans-forbindelse, men for Z/E-nomenklaturen er forbindelsen det der svarer til en cis-forbindelse.
Ved cykliske forbindelser betragter man ringen som atomerne udspænder som et plan, og man orienterer cis og trans i forhold til ringens plan. Z/E-nomenklaturen bruges ikke til cykliske forbindelser. Et molekyle som dette

hedder således trans-cyclopentan-1,2-diol (suffixet ol refererer til den funktionelle gruppe alkohol (-OH). Funktionelle grupper bliver gennemgået i det næste afsnit).
Sidekæder og funktionelle grupper
Sidekæder og funktionelle grupper kan være lidt tricky, fordi de har et indbygget hieraki og de funktionelle grupper kan optræde på sidekæderne. Der et par generelle regler, som man skal have i mente:
Vi starter med et simpelt molekyle:
Proceduren for navngivning er:
Vi prøver et lidt mere kompliceret molekyle:

Hvis vi starter fra en ende af:
For lige at addressere problematikken med flere syregrupper. Hvis der kun er 2, og de sidder på hovedkæden, f.eks. glutarsyren:

så er det helt simpelt:
Vi har nu tre syregrupper, hvoraf en sidder på en sidekæde.
Lad os se på endnu et molekyle, hvor navngivningen kan være lidt tricky:
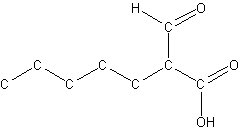
Hvis vi starter fra en ende af:
Dette er hvis man følger reglerne stringent. Mere pragmatisk, og lige så entydigt (og dermed lige så korrekt) er:
Navngivningen af aromatiske forbindelser fungerer efter samme principper som alifatiske og cyckliske forbindelser. Benzen med en enkelt substituent hedder således:
Hvis der er flere substituenter, er det den hovedfunktionelle gruppe der bestemmer nummereringen, og navngivningen følger den normale procedure for navngivning.
En speciel ting der hører til aromatiske forbindelser er brugen af ortho-, meta- og para- i stedet for positionsangivelserne 1, 2 og 3 ved flere substituenter. På skrift forkorter man gerne ortho-, meta- og para- til o-, m- og p-. Bemærk at ortho-, meta- og para- er med kursiv i den kemiske retsskrivning. Ligeledes vil man ofte opleve halvsystematiske navne som f.eks. 3-nitro-toluen fordi methylbenzen har trivialnavnet toluen, og toluen er det navn der bruges mest, f.eks.
- Alifatiske sidekæder navngives ved at give kæden endelsen -yl. For alkaner skiftes -an ud med -yl, mens for alkener og alkyner adderes -yl til hhv. -enyl og -ynyl.
- For ikke alifatiske sidekæder skal man kende det specifikke navn for typen, f.eks. en benzenring hedder en phenyl.
- Næsten alle funktionelle grupper har et navn som præfix og suffix. Præfix er den funktionelle gruppes navn, når den ikke er hovedgruppen. Suffix er gruppens navn, når den er hovedgruppen. Et molekyle kan således kun have ét suffix, men gerne flere præfix.
- Der er til de funktionelle grupper et hieraki, der definerer hvilken gruppe der er den dominerende ved flere funktionelle grupper. Den mest oxiderede funktionelle gruppe er den dominerende.
- Nummereringen af placeringerne skal være således, at den bliver lavest mulig. Den dominerende funktionelle gruppe afgør hvilket carbon der er nummer 1. Den funktionelle gruppe behøver ikke at sidde på nummer 1, men positionen skal have det lavest mulige nummer.
Vi starter med et simpelt molekyle:
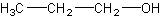
Proceduren for navngivning er:
- Der er 3 carbon og kun enkeltbindinger, så det kommer til at hedde noget med propan (prop = 3 carbon, -an = enkeltbindinger).
- Molekylet indeholder en OH-gruppe, som er en alkohol (se funktionelle grupper). Der er kun den ene funktionelle gruppe, så den bliver den dominerende gruppe og skal skrives som suffix. Den får derfor endelsen -ol. Molekylet kommer så til at hedde noget med propanol.
- Alkoholgruppen sidder på det yderste carbon, hvilket vil være carbon nummer 1 eller nummer 3 afhængig af hvilken ende vi tæller fra. Vi skal have det lavest mulige tal på i navngivningen, så det får positionen 1. Molekylets navn bliver så propan-1-ol. Bemærk: Ikke alle funktionelle grupper behøver en angivelse af position, fordi de kun kan være anbragt ét sted på kæden, f.eks. aldehyder og carboxylsyrer.
Vi prøver et lidt mere kompliceret molekyle:

Hvis vi starter fra en ende af:
- Der er 4 carbon og kun enkeltbindinger i carbonkæden, så det kommer til at hedde noget med butan (but = 4 carbon, -an = enkeltbindinger).
- Molekylet indeholder en OH-gruppe, som er en alkoholgruppe, og en C(=O)OH-gruppe som er en carboxylsyre. Carboxylsyren har den højeste prioritet, så den kommer til at stå som suffix, dvs. navnet bliver noget med syre. Molekylet skal så hedde noget med butansyre.
- Alkoholgruppen er nu nødt til at stå som præfix, dvs. hydroxy. Vi kan nu udvide navnet til hydroxy-butansyre.
- Placeringen af syregruppen definerer hvor carbon nummer 1 er placeret, og syregrupper kan kun være endestillede. Det eneste tidspunkt hvor man ser en syregruppe med andet nummer end 1, er ved flere syregrupper (eksempel kommer længere nede). Alkoholgruppen sidder således på carbon nummer 3. Navnet bliver da 3-hydroxy-butansyre.
For lige at addressere problematikken med flere syregrupper. Hvis der kun er 2, og de sidder på hovedkæden, f.eks. glutarsyren:

så er det helt simpelt:
- Der er 5 carbon og kun enkeltbindinger, så det bliver noget med pentan.
- Der er 2 carboxylsyrer, så vi kan udvide navnet til pentandisyre.
- Det er nødvendigvis kun den ene der kan have nummer et, hvilket betyder at den anden må sidde på nummer 5. På den anden side, er molekylet en alifat, så der er kun to ender hvor carboxylsyrerne kan sidde. Så selv om man kunne få den tanke, at molekylet skulle hedde pentan-1,5-disyre, er det tilstrækkeligt blot med pentandisyre for at have et entydigt navn.

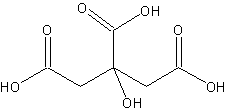
Vi har nu tre syregrupper, hvoraf en sidder på en sidekæde.
- Som altid ser vi efter den længste kæde med flest substituenter. Det er muligt at vælge mellem en disyre med 4 carbon (yderste og midterste syregruppe) eller en disyre med 5 carbon (de 2 yderste syregrupper), så det bliver nødvendigvis de 5 carbon. Molekylet må derfor hedde noget med pentandisyre.
- Den midterste syregruppe (på position 3) bliver nu degraderet til at være sidekæde. Så kommer den til at hedde 3-carboxy, og det fulde navn bliver noget med 3-carboxy-pentandisyre.
- Alkoholgruppen på position 3 kommer også til at figurere som præfix, dvs. hydroxy, og fordi substituenterne listes alfabetisk (efter nummerrækkefølgen) bliver det noget med 3-carboxy-3-hydroxypentandisyre.
- Selv om de to carboxylsyrer kun man sidde endestillet, er der mange der godt kan lide at angive deres nummer, dvs. 3-carboxy-3-hydroxypentan-1,5-disyre. Det er ikke forkert navngivning, det er bare heller ikke strengt nødvenigt
- Den længste kæde med flest substituenter (stamhydridet) er 3 carbon med 3 carboxygrupper på. Molekylet må derfor hedde noget med propan.
- De tre syregrupper bliver nu en specifik navngivet gruppe, dvs. en carboxylsyre (her tricarboxylsyre fordi der er 3 af dem), på propanen, der sidder på positionerne 1, 2 og 3. Molekylet kommer så til at hedde noget med propan-1,2,3-tricarboxylsyre.
- Alkoholgruppen på position 2 kommer til at figurere som præfix, dvs. hydroxy, så navnet bliver 2-hydroxypropan-1,2,3-carboxylsyre.
Lad os se på endnu et molekyle, hvor navngivningen kan være lidt tricky:

Hvis vi starter fra en ende af:
- Den længste carbonkæde er 7 carbon, så man kunne forledes til at tro, at molekylet burde hedde noget med heptan. Men, hvis vi skal følge reglerne stringent, er den længste carbonkæde med flest funktionelle grupper fra carboxylsyren til aldehydet. Hovedkæden bliver således 3 carbon lang, dvs. propan.
- Molekylet indeholder en CHO-gruppe, som er en aldehydgruppe, og en C(=O)OH-gruppe som er en carboxylsyre. Carboxylsyren har den højeste prioritet, så den kommer til at figurere som suffix, dvs. syre. Molekylet skal altså hedde noget med propansyre.
- Aldehydgruppen er nu nødt til at stå som præfix, dvs. oxo. Vi kan nu udvide navnet til oxopropansyre.
- Syregruppen kan kun sidde yderst, og som den højst prioriterede funktionelle gruppe, definerer dette hvor carbon nummer 1 er placeret. Aldehydgruppen sidder således på carbon nummer 3, og navnet bliver da 3-oxopropansyre.
- Den sidste gruppe er alifatisk kæde på 5 carbon, dvs. pentan. Som sidekæde kommer den til at hedde pentyl, og den sidder på position 2. Molekylet kommer så, fordi substituenterne listes alfabetisk, til at hedde 3-oxo-2-pentylpropansyre.
Dette er hvis man følger reglerne stringent. Mere pragmatisk, og lige så entydigt (og dermed lige så korrekt) er:
- Der er to funktionelle grupper, en carboxylsyre og et aldehyd, og af disse er carboxylsyren den funktionelle gruppe med højest prioritet.
- Den længste carbonkæde der sidder på syren er 7 carbon, så molekylet hedder noget med heptansyre.
- Aldehydgruppen er nu nødt til at stå som præfix. Methanal som en sidelæde hedder formyl, så vi kan nu udvide navnet til formylheptansyre.
- Syregruppen kan kun sidde yderst, og som den højst prioriterede funktionelle gruppe, definerer dette hvor carbon nummer 1 er placeret. Aldehydgruppen sidder således på carbon nummer 2, og navnet bliver da 2-formylheptansyre.
Navngivningen af aromatiske forbindelser fungerer efter samme principper som alifatiske og cyckliske forbindelser. Benzen med en enkelt substituent hedder således:
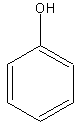
|  |
| Hydroxybenzen | Methylbenzen |
Hvis der er flere substituenter, er det den hovedfunktionelle gruppe der bestemmer nummereringen, og navngivningen følger den normale procedure for navngivning.
En speciel ting der hører til aromatiske forbindelser er brugen af ortho-, meta- og para- i stedet for positionsangivelserne 1, 2 og 3 ved flere substituenter. På skrift forkorter man gerne ortho-, meta- og para- til o-, m- og p-. Bemærk at ortho-, meta- og para- er med kursiv i den kemiske retsskrivning. Ligeledes vil man ofte opleve halvsystematiske navne som f.eks. 3-nitro-toluen fordi methylbenzen har trivialnavnet toluen, og toluen er det navn der bruges mest, f.eks.
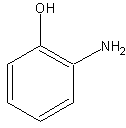 |  | 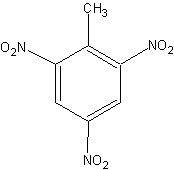 |
| 2-aminohydroxybenzen ortho-aminohydroxy-benzen |
1,3-dimethylbenzen meta-dimethylbenzen m-xylen |
2,4,6-trinitromethylbenzen 2,4,6-trinitrotoluen (TNT) |
N-substituerede aminer og amider
Nitrogenet i aminer og amider tillader flere bindinger. For aminer taler man om sekundære og tertiære aminer, afhængig af om der er 2 eller 3 substituenter på. Man kalder dem også for N-substituerede aminer. For amider har man en orientering i forhold til carbonylgruppen, der er en del af amidgruppen. Her taler man, analogt til aminerne, om N-substituerede amider og sekundære og tertiære amider.
Aminernes navngivning følger de almindelige regler for navngivning med længste kæde med flest substituenter som hovedkæden. Hvis vi starter med en primær amin som ethylamin:

Hvis vi sætter en methylgruppe på nitrogenet, kommer det til at se således ud:

Dette er N-methyl-ethylamin. Sætter vi en methylgruppe mere på, kalder man det N,N'-dimethyl-ethylamin. Hvis der ikke er tvivl om placeringerne, som f.eks. ved triethylamin:
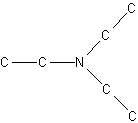
angiver man ikke N,N'.
Analogt til aminerne, kan vi med amiderne starte med ethylamid:
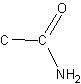
Hvis vi sætter en methylgruppe på nitrogenet, kommer det til at se således ud:
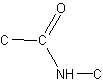
Dette er N-methyl-ethylamid. Sætter vi en methylgruppe mere på, kalder man det N,N'-dimethyl-ethylamid.
Med amider skal man være lidt opmærksom, da amidet har en orientering. Man ser det f.eks. ved dette molekyle:
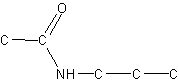
Her er den længste kæde på 3 carbon, men carbonylgruppen, som er en del af amid som funktionel gruppe, sidder på ethyl-kæden, så det bliver til en N-propyl-ethylamid.
Aminernes navngivning følger de almindelige regler for navngivning med længste kæde med flest substituenter som hovedkæden. Hvis vi starter med en primær amin som ethylamin:

Hvis vi sætter en methylgruppe på nitrogenet, kommer det til at se således ud:

Dette er N-methyl-ethylamin. Sætter vi en methylgruppe mere på, kalder man det N,N'-dimethyl-ethylamin. Hvis der ikke er tvivl om placeringerne, som f.eks. ved triethylamin:

angiver man ikke N,N'.
Analogt til aminerne, kan vi med amiderne starte med ethylamid:

Hvis vi sætter en methylgruppe på nitrogenet, kommer det til at se således ud:

Dette er N-methyl-ethylamid. Sætter vi en methylgruppe mere på, kalder man det N,N'-dimethyl-ethylamid.
Med amider skal man være lidt opmærksom, da amidet har en orientering. Man ser det f.eks. ved dette molekyle:

Her er den længste kæde på 3 carbon, men carbonylgruppen, som er en del af amid som funktionel gruppe, sidder på ethyl-kæden, så det bliver til en N-propyl-ethylamid.
Optisk isomeri, R/S-form
Optisk isomeri kræver en 3D-tegning og en rumlig forståelse af et molekyle, hvis man skal kunne se det. Hvis vi ser på pentan-2-ol i en 2D-tegning, ser således ud:
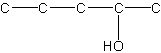
Vi kan se, at carbon i position 2 har fire forskellige substituenter, så der er to optiske isomerer af molekylet. Vi kan ikke se hvilken af de to der er tale om, og det kunne være en racemisk blanding. Det kræver en rumlig angivelse af hvorledes bindingerne er arrangeret, at kunne se hvilken isomer man har. Det kunne f.eks. være sådan her:
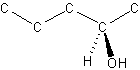
Substituenten med den laveste placering, i dette tilfælde H, kan nu flyttes ind i baggrunden bag det optiske center, så de tre andre substituenter peger ud i rummet mod læseren. Vi kan nu nummerere de tre substituenter der peger ud i rummet efter deres placering i det periodiske system, med den højeste placering som nummer 1:
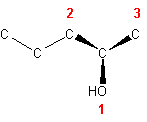
Hvis nummereringen 1 til 3 er med uret, er orienteringen R (Right), og mod uret er orienteringen S (Sinister). Orienteringen er i dette tilfælde, som det kan ses af figuren, mod højre, dvs. en R-form. Stoffet må da være en (R)-pentan-2-ol.
Hvis man arbejder med store og komplekse molekyler, hvor det kan være svært at overskue de optiske centre, eller der er flere optiske centre markerer man dette ved at skrive positionen foran de respektive orienteringer f.eks. (2R,3S)-2,3-dibromopentan.

Vi kan se, at carbon i position 2 har fire forskellige substituenter, så der er to optiske isomerer af molekylet. Vi kan ikke se hvilken af de to der er tale om, og det kunne være en racemisk blanding. Det kræver en rumlig angivelse af hvorledes bindingerne er arrangeret, at kunne se hvilken isomer man har. Det kunne f.eks. være sådan her:

Substituenten med den laveste placering, i dette tilfælde H, kan nu flyttes ind i baggrunden bag det optiske center, så de tre andre substituenter peger ud i rummet mod læseren. Vi kan nu nummerere de tre substituenter der peger ud i rummet efter deres placering i det periodiske system, med den højeste placering som nummer 1:

Hvis nummereringen 1 til 3 er med uret, er orienteringen R (Right), og mod uret er orienteringen S (Sinister). Orienteringen er i dette tilfælde, som det kan ses af figuren, mod højre, dvs. en R-form. Stoffet må da være en (R)-pentan-2-ol.
Hvis man arbejder med store og komplekse molekyler, hvor det kan være svært at overskue de optiske centre, eller der er flere optiske centre markerer man dette ved at skrive positionen foran de respektive orienteringer f.eks. (2R,3S)-2,3-dibromopentan.
Optisk isomeri, L/D-form
Optisk isomeri af denne type bruges kun til monosaccharider, og kræver en markering af hvad der er i planet og ud af planet ligesom i R/S-isomeri. I mod-sætning til R/S-isomeri er der indbygget en orientering i metoden. Når man tegner molekylet, er det i en lodret række med det mest oxiderede carbon øverst. Hvis man skal tegne glucose-molekylet gør man således:
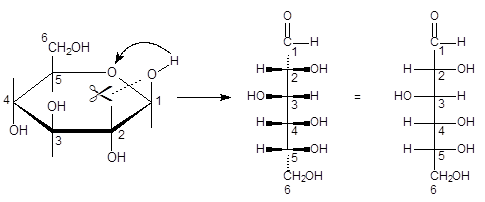
L/D-isomerien afgøres på det optisk aktive carbon med det højeste nummer. Hvis OH-gruppen vender mod højre er det D-formen, og mod venstre er det L-formen. I det viste eksempel er det C(5) der har det højeste nummer, og her vender OH-gruppen mod højre. Der er derfor tale om D-glucose.
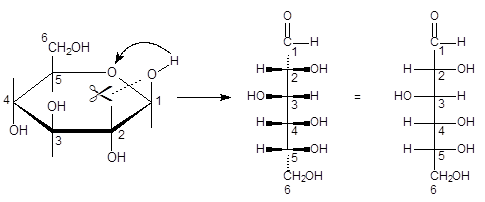
L/D-isomerien afgøres på det optisk aktive carbon med det højeste nummer. Hvis OH-gruppen vender mod højre er det D-formen, og mod venstre er det L-formen. I det viste eksempel er det C(5) der har det højeste nummer, og her vender OH-gruppen mod højre. Der er derfor tale om D-glucose.