
Termisk nedbrydning
Polymerkemi
Hvad går det ud på?
Polymerer nedbrydes over tid som følge af en række påvirkninger, hvoraf en af disse er termiske påvirkninger. Kogt helt ned til det essentielle, handler den termiske nedbrydning om, at de kovalente bindinger brydes pga. temperaturpåvirkninger.
Hvis man betragter en binding mellem to atomer som en fjeder mellem to kugler, vil bindingen vibrere i longitudinale og transversale bevægelser, dvs. i længderetningen og fra side til side. Denne "fjeder" har en trækstyrke, bindingsenergien, og bliver bindingen udsat for træk, der overstiger bindingens brudstyrke, vil bindingen brydes.
For de fleste bindinger vil tilførelsen af energi i form af varme få molekylerne til at bevæge sig mere, og have mere kraft til at bryde de kovalente bindinger. Dette har bl.a. ført til den almindelige misforståelse omkring den terminske nedbrydning, at den følger Arrhenius ligning, dvs. jo varmere det er, desto hurtigere går nedbrydningen, med en fordobling af hastigheden pr. 10 °C som temperaturen stiger.
Overvej lige dette eksempel:
Hvorfor det lige er, at Arrhenius ligning er så misvisende, kommer længere nede. Det er i virkeligheden ikke særligt interessant. Det der er interessant er HVORFOR man har denne forskel, for polymerprodukter anvendes under mange forskellige temperaturforhold, og det er derfor ikke uvæsentligt hvorfor polymererne reagerer så forskelligt ved varierende temperaturpåvirkninger. Der findes polymertyper og blandinger der ikke er så temperaturfølsomme som proteinerne i æg, og der findes en række additiver til polymerer der kan gøre polymeren mere eller mindre følsom overfor temperaturpåvirkninger, så termisk nedbrydning for polymerer er i praksis ikke helt stringent, men mere nogle generelle guidelines med lidt spillerum.
Den korte forklaring på hvorfor man har denne forskel er, at det er fordi polymerkæderne, og hvad der ellers er sammen med dem, påvirker hinanden ved elektrostatiske interaktioner. For at en reaktion kan forløbe, skal man over aktiveringsenergien for reaktionen. Med en katalysator kan man reducere aktiveringsenergien ved at tage en omvej, men der er stadig en aktiveringsenergi der skal overvindes. Jo højere temperatur jo flere aktiveringsenergier kommer man over. Det er ikke nødvendigvis det samme som at der kommer flere reaktionsprodukter eller at polymeren nedbrydes hurtigere. Det kan lige så godt være, at der dannes færre produkter og at et af de dannede produkter fungerer som en inhibitor for nedbrydningen af polymeren.
Så, lad os se på hvordan det i fungerer i praksis.
Hvis man betragter en binding mellem to atomer som en fjeder mellem to kugler, vil bindingen vibrere i longitudinale og transversale bevægelser, dvs. i længderetningen og fra side til side. Denne "fjeder" har en trækstyrke, bindingsenergien, og bliver bindingen udsat for træk, der overstiger bindingens brudstyrke, vil bindingen brydes.
For de fleste bindinger vil tilførelsen af energi i form af varme få molekylerne til at bevæge sig mere, og have mere kraft til at bryde de kovalente bindinger. Dette har bl.a. ført til den almindelige misforståelse omkring den terminske nedbrydning, at den følger Arrhenius ligning, dvs. jo varmere det er, desto hurtigere går nedbrydningen, med en fordobling af hastigheden pr. 10 °C som temperaturen stiger.
Overvej lige dette eksempel:
Et almindeligt hønseæg, placeret ved stuetemperatur i 80 dage, giver et råddent æg. Under en høne, ca. 37 °C i 21 dage, giver en kylling. Otte timer i kogende vand (100 °C) giver et (meget) hårdkogt æg. Ifølge Arrhenius skulle man få det samme resultat.
Hvorfor det lige er, at Arrhenius ligning er så misvisende, kommer længere nede. Det er i virkeligheden ikke særligt interessant. Det der er interessant er HVORFOR man har denne forskel, for polymerprodukter anvendes under mange forskellige temperaturforhold, og det er derfor ikke uvæsentligt hvorfor polymererne reagerer så forskelligt ved varierende temperaturpåvirkninger. Der findes polymertyper og blandinger der ikke er så temperaturfølsomme som proteinerne i æg, og der findes en række additiver til polymerer der kan gøre polymeren mere eller mindre følsom overfor temperaturpåvirkninger, så termisk nedbrydning for polymerer er i praksis ikke helt stringent, men mere nogle generelle guidelines med lidt spillerum.
Den korte forklaring på hvorfor man har denne forskel er, at det er fordi polymerkæderne, og hvad der ellers er sammen med dem, påvirker hinanden ved elektrostatiske interaktioner. For at en reaktion kan forløbe, skal man over aktiveringsenergien for reaktionen. Med en katalysator kan man reducere aktiveringsenergien ved at tage en omvej, men der er stadig en aktiveringsenergi der skal overvindes. Jo højere temperatur jo flere aktiveringsenergier kommer man over. Det er ikke nødvendigvis det samme som at der kommer flere reaktionsprodukter eller at polymeren nedbrydes hurtigere. Det kan lige så godt være, at der dannes færre produkter og at et af de dannede produkter fungerer som en inhibitor for nedbrydningen af polymeren.
Så, lad os se på hvordan det i fungerer i praksis.
Konformationsændringer
Polymerens konformation, dvs. den tredimensionelle struktur (arkitektur), er en af de vigtige faktorer i polymerers stabilitet. Sammenhængen er kompleks og kan være svær at gennemskue.
For alle kemiske forbindelser har man både en energetisk og en sterisk favorabel struktur. Strukturen behøver ikke være ordnet eller blot delvist ordnet, dvs. helt eller delvist krystallinsk, amorf (eller random coil om man vil) er også en struktur. De to strukturer kan være det samme, men det er langt fra altid tilfældet. Man kan ligeledes også sagtens have flere energetisk favorable strukturer for et materiale, således at polymeren skifter konformation flere gange med stigende og faldende temperaturer.
Hvis de to strukturer er forskellige, er det den energisk favorable struktur som materialet antager, indtil man når det energiniveau (dvs. temperaturen), hvor materialet kan antage den sterisk favorable konformation.
Ud over temperaturen til at påvirke konformationen, har man også effekterne af eventuelle additiver. Dette er f.eks. to konformationer af DNA (a- og b-form, hhv. venstre og højre), hvor forskellen alene er en effekt af vandmængde:
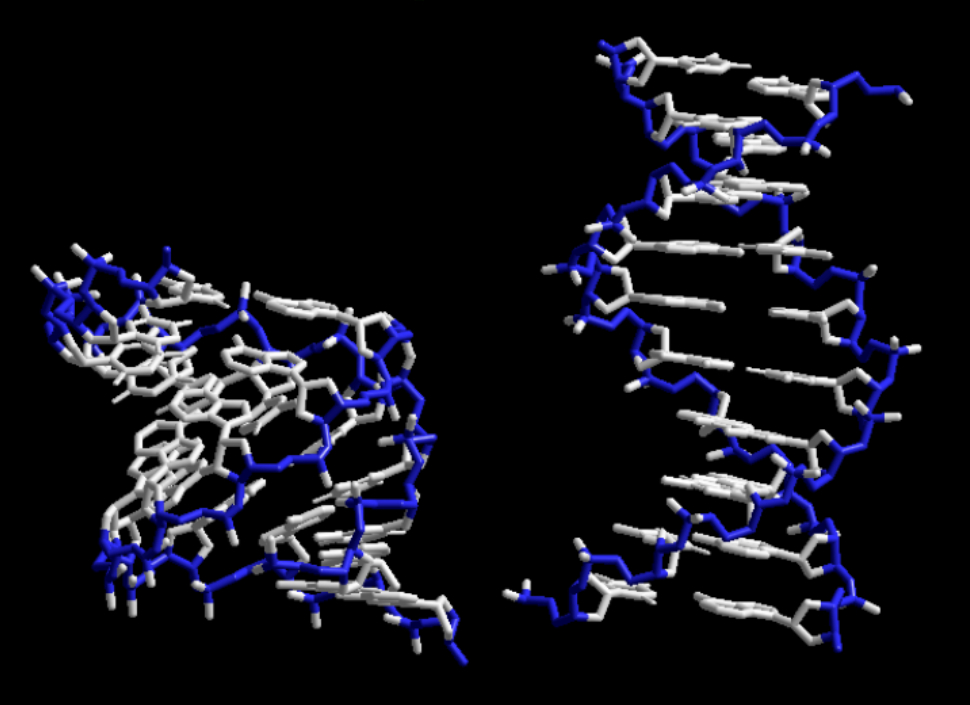
Har man de rette solventforhold, kan man få drejet helixformationen den anden vej rundt. Dette hedder Z-DNA.
Selv rene plast- og gummityper er ikke helt rene, idet de indeholder forskellige mængder antioxidanter og UV-stabilisatorer, og ved eksponering for atmosfærisk luft, vil de også indeholde forskellige mængder vand fra ligevægten med luftens fugtighed. Dette vil i en eller anden grad kunne påvirke konformationen ved en given temperatur.
Ved direkte kontakt med kemikalier, f.eks.
Polymerens konformation lægger nogle spændinger på bindingerne i polymeren på samme måde som hvis man bøjer eller strækker et stykke metal. Forskellige konformationer giver forskellige spændinger og fordeling af spændingerne langs polymerkæden. Man ved f.eks. at i proteiner er amidbindingerne ikke nødvendigvis de teoretiske 180°, men svinger ±20°, hvilket giver nogle spændinger i amidbindingerne. Polariseringer af bindinger som følge af additiver vil give en svagere kovalent binding. Hydrogenbindinger kan omvendt virke stabiliserende og forstærkende. Det samme kan krystallinitet og tværbindinger (vulkaniseringer) i polymererne. Højere temperaturer giver større og/eller hurtigere svingninger i bindingerne.
Der findes områder på polymerkæderne, som fra naturens hånd er svagere end andre, altså strukturelle svagheder i polymerens arkitektur. Disse kaldes hotspots. Man skal her være opmærksom på, at hotspots for termiske nedbrydninger ikke nødvendigvis er det samme som f.eks. materialets hotspots for UV-nedbrydning eller andre påvirkninger.
For at en reaktion kan forløbe, skal man over aktiveringsenergien for reaktionen. Med en katalysator kan man reducere aktiveringsenergien ved at tage en omvej, men der er stadig en aktiveringsenergi der skal overvindes. Jo højere temperatur jo flere aktiveringsenergier kommer man over. Det er ikke nødvendigvis det samme som at der kommer flere reaktionsprodukter eller at polymeren nedbrydes hurtigere. Det kan lige så godt være, at der dannes færre produkter og at et af de dannede produkter fungerer som en inhibitor for nedbrydningen af polymeren.
For alle kemiske forbindelser har man både en energetisk og en sterisk favorabel struktur. Strukturen behøver ikke være ordnet eller blot delvist ordnet, dvs. helt eller delvist krystallinsk, amorf (eller random coil om man vil) er også en struktur. De to strukturer kan være det samme, men det er langt fra altid tilfældet. Man kan ligeledes også sagtens have flere energetisk favorable strukturer for et materiale, således at polymeren skifter konformation flere gange med stigende og faldende temperaturer.
Hvis de to strukturer er forskellige, er det den energisk favorable struktur som materialet antager, indtil man når det energiniveau (dvs. temperaturen), hvor materialet kan antage den sterisk favorable konformation.
Ud over temperaturen til at påvirke konformationen, har man også effekterne af eventuelle additiver. Dette er f.eks. to konformationer af DNA (a- og b-form, hhv. venstre og højre), hvor forskellen alene er en effekt af vandmængde:

Har man de rette solventforhold, kan man få drejet helixformationen den anden vej rundt. Dette hedder Z-DNA.
Selv rene plast- og gummityper er ikke helt rene, idet de indeholder forskellige mængder antioxidanter og UV-stabilisatorer, og ved eksponering for atmosfærisk luft, vil de også indeholde forskellige mængder vand fra ligevægten med luftens fugtighed. Dette vil i en eller anden grad kunne påvirke konformationen ved en given temperatur.
Ved direkte kontakt med kemikalier, f.eks.
- detergenter og vand ved vask, f.eks. tøjvask, hårvask og tandbørstning
- fødevarer i beholdere, f.eks. mælkeprodukter, olier og eddike
- lipider fra huden ved kontakt med f.eks. håndtag, smykker, høreapparater og ear phones
- kemikalier fra kosmetik og hudplejeprodukter på huden mod f.eks. håndtag, smykker, høreapparater og ear phones
Polymerens konformation lægger nogle spændinger på bindingerne i polymeren på samme måde som hvis man bøjer eller strækker et stykke metal. Forskellige konformationer giver forskellige spændinger og fordeling af spændingerne langs polymerkæden. Man ved f.eks. at i proteiner er amidbindingerne ikke nødvendigvis de teoretiske 180°, men svinger ±20°, hvilket giver nogle spændinger i amidbindingerne. Polariseringer af bindinger som følge af additiver vil give en svagere kovalent binding. Hydrogenbindinger kan omvendt virke stabiliserende og forstærkende. Det samme kan krystallinitet og tværbindinger (vulkaniseringer) i polymererne. Højere temperaturer giver større og/eller hurtigere svingninger i bindingerne.
Der findes områder på polymerkæderne, som fra naturens hånd er svagere end andre, altså strukturelle svagheder i polymerens arkitektur. Disse kaldes hotspots. Man skal her være opmærksom på, at hotspots for termiske nedbrydninger ikke nødvendigvis er det samme som f.eks. materialets hotspots for UV-nedbrydning eller andre påvirkninger.
For at en reaktion kan forløbe, skal man over aktiveringsenergien for reaktionen. Med en katalysator kan man reducere aktiveringsenergien ved at tage en omvej, men der er stadig en aktiveringsenergi der skal overvindes. Jo højere temperatur jo flere aktiveringsenergier kommer man over. Det er ikke nødvendigvis det samme som at der kommer flere reaktionsprodukter eller at polymeren nedbrydes hurtigere. Det kan lige så godt være, at der dannes færre produkter og at et af de dannede produkter fungerer som en inhibitor for nedbrydningen af polymeren.
Backbone og kemiske angrebspunkter
Kemiske gruppers reaktivitet er et kardinalpunkt når det kommer til stabilitet. Især funktionelle grupper i polymerens backbone er kritiske, da kædelængden er afgørende for bl.a. materialestyrken, kohesionen og viskoelastiske egenskaber.
Hvis man ser på disse tre polymerer:

Polyethylen (PE)

Polyethylenglycol (PEG)
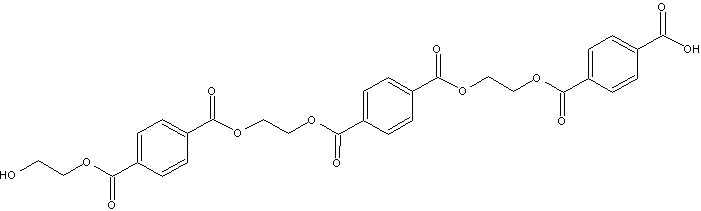
Poly(ethylen terephthalat) (PET)
så har polyethylenen ingen funktionelle grupper i backbone, og er derfor ikke særlig modtagelig for kemikalieangreb, uanset temperaturerne.
Polyethylenglycolen (PEG) derimod vil være modtagelig for hydrolyse ved tilstedeværelsen af vand, under de rette forhold. I vand ved stuetemperatur er PEG en meget stabil polymer, men høje temperaturer eller f.eks. syre til at katalysere processen, vil give hydrolysering af etherbindingerne. Man kunne så forvente, at polypropylenglycol (PPG) ville følge dette mønster, men PPG er uopløselig i vand, hvilket betyder, at vandoptaget er forsvindende lille, uden et co-solvent, og sandsynligheden for hydrolyse tilsvarende mindre.
Polyamider og polyestre hydrolyseres allerede ved stuetemperatur. For både estre og amider, er kondensationsreaktionen der danner dem, i virkeligheden en ligevægt, hvilket betyder, at ved eksponering for vand vil ligevægten forskydes til venstre mod syren og alkoholen/aminen. Alkaliske forhold, som f.eks. havmiljøer, øger reaktionshastigheden, og det samme gør stigende temperaturer.
Funktionelle sidekæder er også kritiske, men her er grunden indirekte. Når sidekædernes ændres eller fjernes, f.eks. en deacetylering af EVA (polyethyl vinylacetat), påvirker det polymerens konformation, hvilket kan gøre backbone sårbart for nedbrydning eller på anden måde ændre polymerens egenskaber.
Der er ikke et entydigt svar på hvilke funktionelle grupper der er mest stabile over for termiske nedbrydninger. Man skal her kende polymerens arkitektur og konformation og vide hvad de bliver eksponeret for, for at kunne forudsige materialets stabilitet. I praksis er dette så komplekst, at man nødt til at bestemme stabiliteten eksperimentelt, hvilket også er det man gør ved f.eks. produktudvikling, og man ser netop, at materialevalg til produkter ofte er baseret på de materialer man har erfaring for fungerer, for at reducere mængden af test ved produktudvikling.
Hvis man ser på disse tre polymerer:

Polyethylen (PE)

Polyethylenglycol (PEG)

Poly(ethylen terephthalat) (PET)
så har polyethylenen ingen funktionelle grupper i backbone, og er derfor ikke særlig modtagelig for kemikalieangreb, uanset temperaturerne.
Polyethylenglycolen (PEG) derimod vil være modtagelig for hydrolyse ved tilstedeværelsen af vand, under de rette forhold. I vand ved stuetemperatur er PEG en meget stabil polymer, men høje temperaturer eller f.eks. syre til at katalysere processen, vil give hydrolysering af etherbindingerne. Man kunne så forvente, at polypropylenglycol (PPG) ville følge dette mønster, men PPG er uopløselig i vand, hvilket betyder, at vandoptaget er forsvindende lille, uden et co-solvent, og sandsynligheden for hydrolyse tilsvarende mindre.
Polyamider og polyestre hydrolyseres allerede ved stuetemperatur. For både estre og amider, er kondensationsreaktionen der danner dem, i virkeligheden en ligevægt, hvilket betyder, at ved eksponering for vand vil ligevægten forskydes til venstre mod syren og alkoholen/aminen. Alkaliske forhold, som f.eks. havmiljøer, øger reaktionshastigheden, og det samme gør stigende temperaturer.
Funktionelle sidekæder er også kritiske, men her er grunden indirekte. Når sidekædernes ændres eller fjernes, f.eks. en deacetylering af EVA (polyethyl vinylacetat), påvirker det polymerens konformation, hvilket kan gøre backbone sårbart for nedbrydning eller på anden måde ændre polymerens egenskaber.
Der er ikke et entydigt svar på hvilke funktionelle grupper der er mest stabile over for termiske nedbrydninger. Man skal her kende polymerens arkitektur og konformation og vide hvad de bliver eksponeret for, for at kunne forudsige materialets stabilitet. I praksis er dette så komplekst, at man nødt til at bestemme stabiliteten eksperimentelt, hvilket også er det man gør ved f.eks. produktudvikling, og man ser netop, at materialevalg til produkter ofte er baseret på de materialer man har erfaring for fungerer, for at reducere mængden af test ved produktudvikling.
Fyldstoffer og interfaces
Man har til polymerer en række fyldstoffer til forskellige formål, f.eks. styrke, hårdhed og brandtekniske egenskaber. Disse fyldstoffer giver en heterogen polymerblanding, dvs. materialet bliver en komposit, og man står med to potentielle problemer i forhold til termisk nedbrydning:
For at sikre et ordentligt interface mellem fyldstof og polymer, har man på mange fyldstoffer en kovalent bundet overflademodificering (kaldes også en graftet overflademodificering). Inden for glas- og kulfiberkompositter kalder man denne graftede overflade for "sizing", mens man for calcium- og og silikapartikler blot kalder det "coatning" eller "overflademodificering". Ud over at man skal sikre sig, at coatningen er termostabil, så den bliver ved med at være på overfladen, skal man også være obs på eventuelle temperaturafhængigheder for de elektrostatiske interaktioner mellem polymermatricen og fyldstoffets overflade.
Termisk stabilitet af fyldstoffet er mest af interesse for polymerfibre og brandhæmmende mineraler som ATH (aluminium trihydroxid). Ved opvarmning afgiver ATH vand, hvilket er den brandhæmmende egenskab, men dette begynder allerede ved 180 °C, hvilket er lavere end procestemperaturerne for produktionen af en del plast- og gummityper. Polymerfibrene følger den termiske nedbrydning for den pågældende polymertype.
Hvis man har materialer der anvendes i områder med store eller hurtige temperatursvingninger, skal være obs på forskelle i forskelle i materialernes termiske ekspansionskoefficienter. Hvis ikke det ene af de to materialer er fleksibelt nok til at kunne absorbere forskellene i volumenændringer ved temperatursvingninger, får man nogle spændinger i interfasen, som kan få polymeren til at slippe fyldstoffet.
- Interface mellem polymermatricen og fyldstoffet
- Termisk stabilitet af fyldstoffet
For at sikre et ordentligt interface mellem fyldstof og polymer, har man på mange fyldstoffer en kovalent bundet overflademodificering (kaldes også en graftet overflademodificering). Inden for glas- og kulfiberkompositter kalder man denne graftede overflade for "sizing", mens man for calcium- og og silikapartikler blot kalder det "coatning" eller "overflademodificering". Ud over at man skal sikre sig, at coatningen er termostabil, så den bliver ved med at være på overfladen, skal man også være obs på eventuelle temperaturafhængigheder for de elektrostatiske interaktioner mellem polymermatricen og fyldstoffets overflade.
Termisk stabilitet af fyldstoffet er mest af interesse for polymerfibre og brandhæmmende mineraler som ATH (aluminium trihydroxid). Ved opvarmning afgiver ATH vand, hvilket er den brandhæmmende egenskab, men dette begynder allerede ved 180 °C, hvilket er lavere end procestemperaturerne for produktionen af en del plast- og gummityper. Polymerfibrene følger den termiske nedbrydning for den pågældende polymertype.
Hvis man har materialer der anvendes i områder med store eller hurtige temperatursvingninger, skal være obs på forskelle i forskelle i materialernes termiske ekspansionskoefficienter. Hvis ikke det ene af de to materialer er fleksibelt nok til at kunne absorbere forskellene i volumenændringer ved temperatursvingninger, får man nogle spændinger i interfasen, som kan få polymeren til at slippe fyldstoffet.
Arrhenius ligning
Hvad er Arrhenius ligning og hvorfor er det så det går galt ved brugen af den?
Arrhenius ligning er en matematisk model, som man bruger til beregninger af reaktioners aktiveringsenergi. Ligningen ser således ud:
R er en naturkonstant, og k0 og Ea er reaktionsspecifikke konstanter (hhv. hastighedskonstant og aktiveringsenergi). k og T er variablerne, når man kører en reaktion ved to forskellige temperaturer for at bestemme reaktionens aktiveringsenergi. Fordoblingen pr. 10 °C, som man arbejder med, kommer af matematikken i eksponentialligningen hvor temperaturen T stiger til (T + 10 °C).
Helt grundliggende går det galt fordi ligningen forudsætter at det er den samme reaktion der forløber ved to forskellige temperaturer. Dette er kun korrekt inden for et relativt snævert temperaturinterval, og intervallet bliver mindre og mindre med stigende kompleksitet i reaktionsblandingen. Fordi fordoblingen af reaktionshastigheden pr. 10 °C er en effekt af matematikken, kan man heller ikke have et tilpasset fit, f.eks. en fordobling pr. 9 °C eller 2,5 gange hastighedsforøgelse pr. 10 °C. Har man ikke en fordobling af reaktionshastigheden pr. 10 °C, måler man med sikkerhed på to forskellige reaktioner ved de to temperaturer.
Arrhenius ligning er en matematisk model, som man bruger til beregninger af reaktioners aktiveringsenergi. Ligningen ser således ud:
k = k0 · 10
| -Ea |
| R · T |
R er en naturkonstant, og k0 og Ea er reaktionsspecifikke konstanter (hhv. hastighedskonstant og aktiveringsenergi). k og T er variablerne, når man kører en reaktion ved to forskellige temperaturer for at bestemme reaktionens aktiveringsenergi. Fordoblingen pr. 10 °C, som man arbejder med, kommer af matematikken i eksponentialligningen hvor temperaturen T stiger til (T + 10 °C).
Helt grundliggende går det galt fordi ligningen forudsætter at det er den samme reaktion der forløber ved to forskellige temperaturer. Dette er kun korrekt inden for et relativt snævert temperaturinterval, og intervallet bliver mindre og mindre med stigende kompleksitet i reaktionsblandingen. Fordi fordoblingen af reaktionshastigheden pr. 10 °C er en effekt af matematikken, kan man heller ikke have et tilpasset fit, f.eks. en fordobling pr. 9 °C eller 2,5 gange hastighedsforøgelse pr. 10 °C. Har man ikke en fordobling af reaktionshastigheden pr. 10 °C, måler man med sikkerhed på to forskellige reaktioner ved de to temperaturer.